اثر سطح بر سرعت واکنش
در این طرح درس اثر سطح ماده بر سرعت واکنش بررسی می شود که مواد واکنش دهنده جامد، مایع یا گاز است و کاتالیزور واکنش، جامد است.
چه اتفاقی می افتد؟
در حالتی که ماده خیلی ریز باشد، واکنش سریع تر اتفاق می افتد، به طور معمول واکنش یک پودر جامد نسبت به واکنش همان مقدار ماده اما به صورت توده (ماده متخلخل) سریع تر است. چون پودر دارای سطح بیشتری نسبت به توده ماده است.
اگر واکنش یک نمونه جامد با نمونه گازی شکل را در نظر بگیرید واکنش گاز با نمونه توده ای جامد به خوبی وقتی نمونه به صورت پودر است پیش نمی رود چون گاز به خوبی نمی تواند در نمونه توده ای نفوذ کند. مثلا نمونه توده ای (کپه ای) منیزیم نسبت به نمونه نواری آن تمایل کمتری برای سوختن دارد.
در زیر مثال هایی بیان می کنیم تا مطلب فوق را بهتر درک کنید.
کربنات کلسیم و اسید هیدروکلریک
در آزمایشگاه پودر کربنات کلسیم با اسید هیدروکلریک رقیق شده سریع تر واکنش می دهد تا وقتی که همان مقدار از کربنات کلیسم به صورت سنگ مرمر یا سنگ آهک باشد.
 |
تجزیه کاتالیزوری از پراکسید هیدروژن
تجزیه کاتالیزوری از پراکسید هیدروژن یکی دیگر از واکنش های آشنای آزمایشگاه است. اکسید منگنز (IV) اغلب به عنوان کاتالیزور استفاده می شود. در واکنش تجزیه زیر اگر کاتالیزور به صورت پودر باشد اکسیژن سریع تر آزاد می شود در مقایسه با وقتی که کاتالیزور به صورت توده باشد.
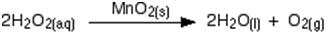 |
مبدل های کاتالیزوری
مبدل های کاتالیزوری از قلزاتی مثل پلاتین، پلادیوم و رادیوم برای تبدیل ترکیبات سمی در اگزوز وسایل نقلیه استفاده می کنند تا مواد سمی را به مواد با ضرر کمتر تبدیل کنند مثلا در واکنش زیر هم مونوکسیدکربن و هم اکسید نیتروزن هر دو حذف می شوند.
 |
از آن جا که گازهای خروجی از اگزوز مدت زمان بسیا رکوتاهی با کاتالیزور در تماس اند، واکنش باید بسیار سریع اتفاق بیافتد. فلزات بسیار گران قیمتی به عنوان کاتالیزور استفاده می شوند، این فلزات به صورت یک لایه نازک روی ساختار لانه زنبوری سرامیکی به منظور به داکثر رساندن سطح تماس موثر قرار داده می شوند.
فقط زمانی یک واکنش اتفاق می افتد که ذرات گاز یا مایع با ذرات جامد برخورد کنند با افزایش سطح جامد احتمال این که برخورد رخ دهد، بیشتر می شود. واکنش بین فلز منیزیم و یک اسید رقیق مانند اسید هیدروکلریک را در نظر بگیرید، واکنش شامل برخورد بین اتم های منیزیم و یون های هیدروژن است:
 |
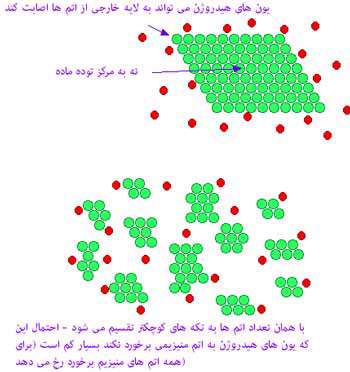
توضیح عکس
هیدروژن می تواند به لایه خارجی از اتم ها اصابت کند نه به مرکز توده ماده
با همان تعداد اتم ها به تکه های کوچکتر تقسیم می شود، احتمال این که یون های هیدروژن به اتم منیزیمی برخورد نکند بسیار کم است (برای همه اتم های منیزیم برخورد رخ می دهد)
افزایش تعداد برخورد در هر ثانیه سرعت واکنش را افزایش می دهد
مسابقه وبلاگ برتر ماه
نظرات شما عزیزان:
موضوعات مرتبط: مطالب علمی ، ،
برچسبها:






 آمار
وب سایت:
آمار
وب سایت:

